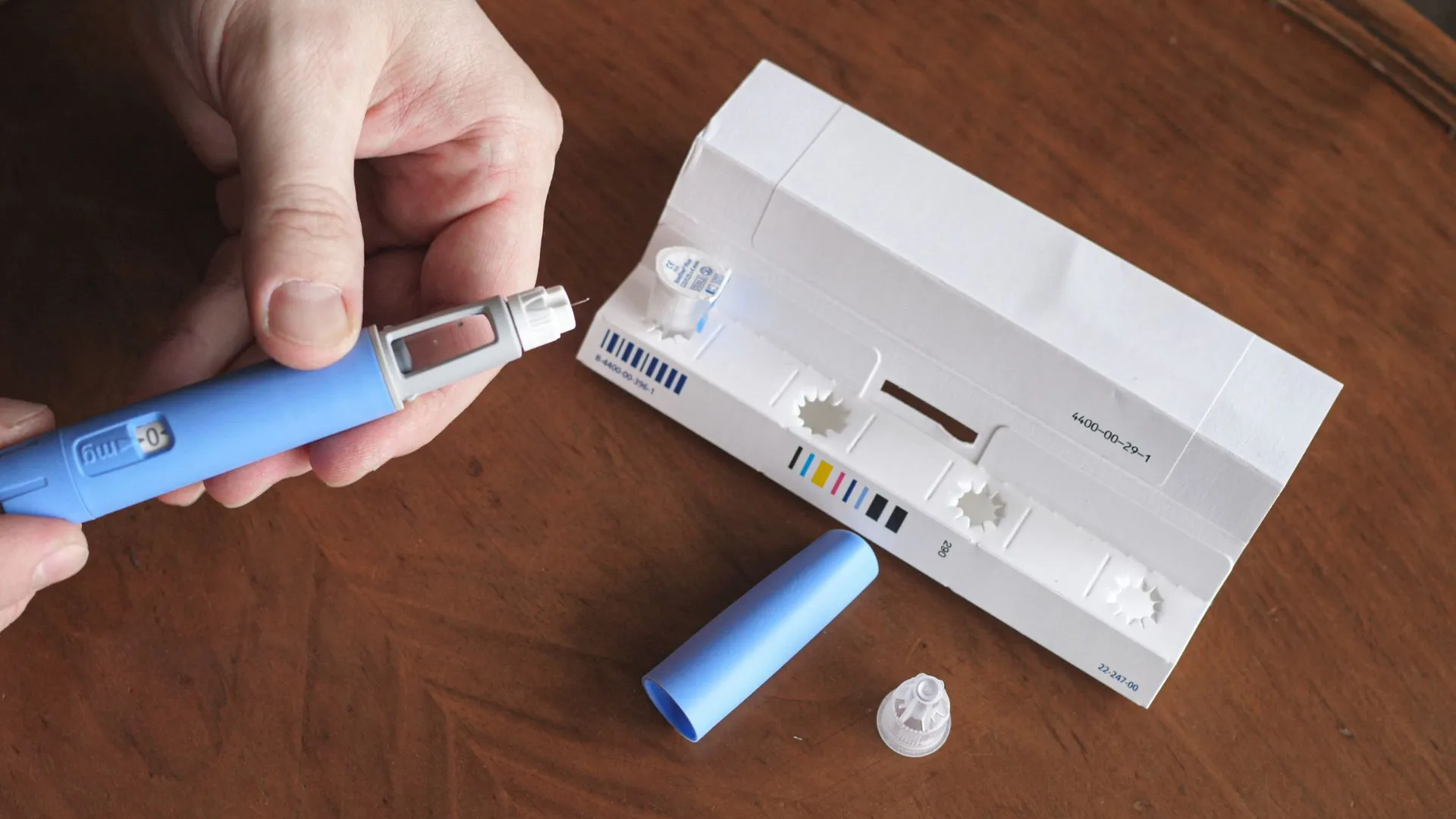
A Agência Nacional de Vigilância Sanitária (Anvisa) publicou uma nova decisão que proíbe a manipulação dos medicamentos Ozempic e Wegovy no Brasil. Esses remédios, indicados para diabetes e perda de peso, pertencem à classe dos análogos de GLP-1. A atualização das regras foi divulgada no Diário Oficial da União (DOU) nesta segunda-feira.
PARTICIPE DO NOSSO GRUPO NO WHATSAPP E RECEBA NOTÍCIAS
No documento, a Anvisa determina que a importação de ingredientes farmacêuticos ativos (IFA) desses análogos obtidos por processo biotecnológico só será permitida de fabricantes que tenham registro na agência.
Atualmente, a Novo Nordisk, laboratório dinamarquês responsável pelo desenvolvimento das canetas Ozempic e Wegovy, é a única empresa com registro para o produto no Brasil.
Por outro lado, a importação dos IFAs obtidos por síntese química continua autorizada, desde que exista um medicamento registrado na Anvisa com a molécula correspondente.
Veja também
PRF apreende quase 300 kg de maconha em SC em apenas 24 horas
SAMU Aeromédico completa 219 missões no Meio-Oeste e reforça agilidade no transporte de pacientes
No entanto, conforme esclarece a Novo Nordisk, “não existe semaglutida (princípio ativo dos medicamentos) de origem sintética registrada no Brasil, apenas por processo biotecnológico”.
Portanto, na prática, a medida restringe a manipulação dos remédios no país, limitando a importação à Novo Nordisk.
O laboratório reforça: “Atualmente, não há nenhum medicamento à base de semaglutida sintética registrado no Brasil, o que torna qualquer manipulação da substância, independentemente da origem (biológica e sintética), irregular e ilegal, por não possuir respaldo técnico ou sanitário. Nesse caso, não há garantia de que a substância manipulada seja segura ou eficaz”.
Para a empresa, essa decisão é “uma camada de proteção contra os riscos de produtos manipulados de forma ilegítima”. A produção da semaglutida biológica é complexa e exige padrões rigorosos.
“O processo utiliza células vivas como ‘fábricas naturais’ para construir a molécula de forma precisa e segura, sendo a que mais se assemelha ao hormônio humano”, explica.
No despacho, a Anvisa destaca que “a manipulação desses IFAs envolve uma alta complexidade farmacotécnica e risco sanitário elevado, especialmente em formas estéreis injetáveis”. O órgão ainda ressalta a “complexidade analítica necessária para garantir a identidade, pureza, potência e estabilidade dos referidos IFAs”.
Restrições à manipulação
Antes da decisão, entidades médicas brasileiras já haviam solicitado restrições à manipulação desses análogos de GLP-1.
Em fevereiro, a Sociedade Brasileira de Endocrinologia e Metabologia (SBEM), a Sociedade Brasileira de Diabetes (SBD) e a Associação Brasileira para o Estudo da Obesidade e Síndrome Metabólica (Abeso) emitiram nota conjunta.
O documento alerta que as versões manipuladas não seguem os mesmos processos rigorosos de fabricação.
Segundo a nota, “o uso de versões alternativas ou manipuladas dessas moléculas tem se tornado uma prática crescente, preocupante e perigosa, carecendo de bases científicas e regulatórias que garantam a eficácia, segurança, pureza e estabilidade do produto, expondo os usuários a sérios riscos à saúde”. Ainda afirmam que esses produtos “não passam pelos testes de bioequivalência necessários, tornando impossível prever seus efeitos no corpo humano”.
O documento também cita casos documentados pela Food and Drug Administration (FDA), órgão regulador dos Estados Unidos. Segundo o FDA, produtos manipulados podem conter doses superiores ou inferiores ao recomendado, contaminações ou substituições por outras substâncias, trazendo riscos significativos à saúde dos consumidores.
Manipulação de medicamentos
No Brasil, a Anvisa permite a manipulação de medicamentos registrados para situações específicas, como dosagens ou apresentações que não estão disponíveis comercialmente.
Contudo, as farmácias de manipulação não podem manter estoques ou divulgar publicidade, devendo preparar o medicamento apenas mediante prescrição médica.
Como a semaglutida e tirzepatida ainda são protegidas por patente, não existem versões genéricas autorizadas no país.
Apesar disso, algumas farmácias de manipulação têm se aproveitado da popularidade dos remédios, oferecendo produtos supostamente equivalentes a preços mais baixos, o que reforça os riscos apontados pelas autoridades sanitárias.