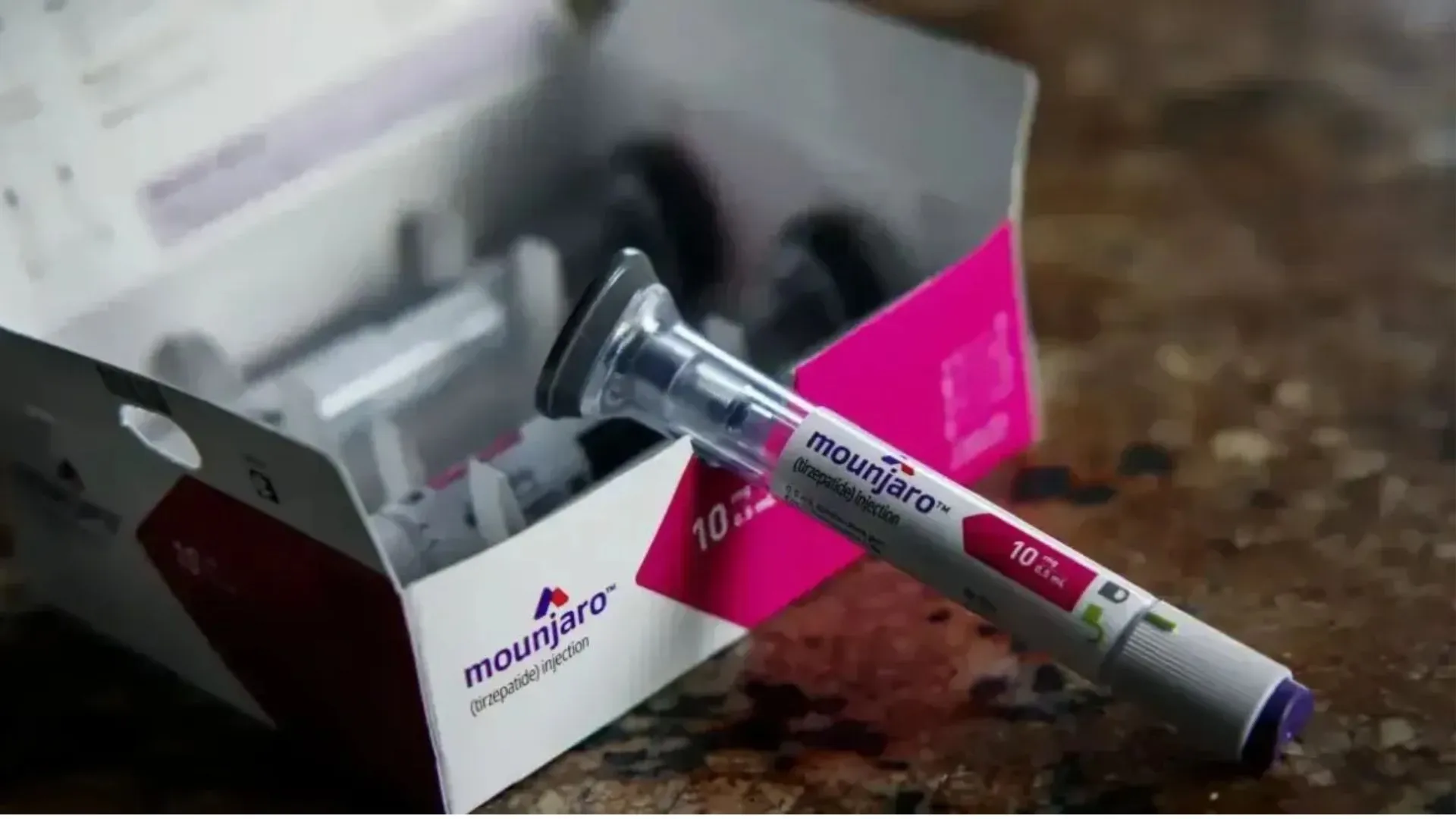
A Agência Nacional de Vigilância Sanitária (Anvisa) aprovou um novo formato do Mounjaro, medicamento indicado para o tratamento do diabetes tipo 2. A confirmação foi publicada no Diário Oficial da União nesta quarta-feira (18), trazendo uma importante inovação para pacientes que dependem da medicação.
PARTICIPE DO NOSSO GRUPO NO WHATSAPP E RECEBA NOTÍCIAS
Diferente do modelo tradicional, que é descartável após cada uso, a nova apresentação, chamada Mounjaro Multidose, foi desenvolvida para que o paciente utilize uma única caneta aplicadora em múltiplas doses, proporcionando mais praticidade e reduzindo o desperdício de material médico.
Registro e dosagens aprovadas
Conforme a Resolução-RE nº 1.041, da Gerência-Geral de Medicamentos da Anvisa, o registro foi concedido à farmacêutica Eli Lilly do Brasil, para o medicamento à base de tirzepatida.
Veja também
Videira conquista 8 medalhas na etapa microrregional dos JASTI e garante vaga no estadual
Câmara aprova lei que define percentual mínimo de cacau em chocolates
A aprovação da Anvisa abrange seis dosagens diferentes, distribuídas em solução injetável para aplicação subcutânea, com validade do registro de 24 meses:
- 4,17 mg/mL
- 8,33 mg/mL
- 12,5 mg/mL
- 16,7 mg/mL
- 20,8 mg/mL
- 25 mg/mL
Principais mudanças e benefícios
A grande inovação do Mounjaro Multidose está no formato: uma única caneta pode ser utilizada em várias aplicações, tornando o tratamento mais prático e eficiente para pacientes que precisam de doses contínuas.
Na prática, a tirzepatida atua nos hormônios responsáveis pelo controle da glicose e do apetite, ajudando no gerenciamento do diabetes tipo 2.
Segundo o Ministério da Saúde e a Anvisa, a medicação deve ser usada em conjunto com dieta de baixa caloria e aumento da atividade física, contribuindo para controle crônico do peso, perda de peso e manutenção em condições específicas.
Essa novidade representa um avanço importante no tratamento do diabetes tipo 2, oferecendo maior conforto ao paciente e garantindo a eficácia já reconhecida do Mounjaro.